一项发表于《核医学杂志》的最新研究,为癌症的精准治疗提供了关键科学依据。2026年3月,美国宾夕法尼亚大学的研究团队利用新型放射性药物,系统揭示了靶向α疗法的核心规律:用于治疗的放射性核素,在癌细胞内的位置距离遗传物质DNA越近,其“定点清除”的杀伤效率就越高。该研究首次通过精确的定量模型证实,将攻击“弹头”直接投送至DNA附近,能最大化其疗效,其中α粒子衰变时产生的“反冲核”起到了重要的额外杀伤作用。
研究团队巧妙地设计了一套“追踪-定位”系统。他们改造了癌细胞,让一种能与特定药物结合的靶点蛋白,被精确地分别安置在细胞的DNA、细胞核、细胞质和细胞膜等不同位置。随后,使用一种能携带放射性核素砹-211、并专门针对该靶点的药物进行治疗。结果清晰显示,当药物结合在DNA或细胞核内的靶点上时,仅需极少量的放射性衰变就足以杀死半数癌细胞,效率远高于结合在细胞质或细胞膜上。即便考虑几何因素进行剂量校准,DNA附近的杀伤优势依然显著,这强力证明了“近DNA攻击”的额外效果。
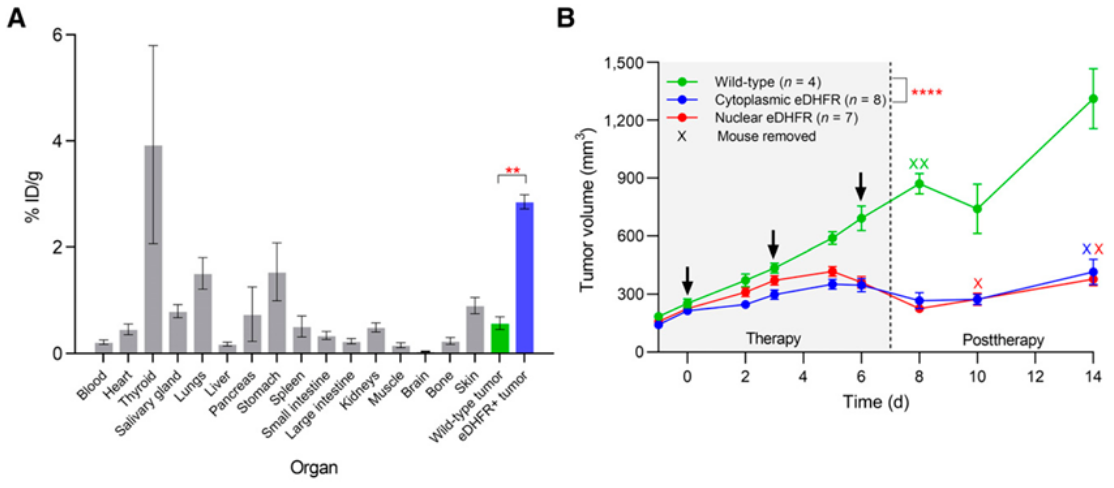
尽管在体外细胞实验中优势明显,但该策略在动物体内的肿瘤模型中遭遇了复杂情况。研究显示,靶向药物能有效富集在特定肿瘤中并抑制其生长,但“核内”与“胞质内”靶向的抑瘤效果差异却不显著。这提示,在真实的实体肿瘤微环境中,药物输送、分布不均等因素可能掩盖了亚细胞定位的精细优势。然而,这一突破性发现对于清除血液中的循环肿瘤细胞或微小的早期转移灶,具有重大的指导价值,为开发下一代高效、低毒的靶向放射性疗法指明了“精准投送”的优化方向。