在这项研究中,我们采用177Lu-AuNPs(β-粒子发射核素177Lu标记23±3 nm金纳米颗粒(AuNPs))通过对流增强递送(CED)的方式来治疗NRG小鼠原位U251-Luc人多形性胶质母细胞瘤(GBM);利用细胞克隆存活法研究了177Lu-AuNPs (0 ~ 2.0 MBq, 4 × 1011 AuNPs)对U251-Luc细胞的体外细胞毒性;通过γ - h2ax共聚焦免疫荧光显微镜检测由177Lu β-粒子发射而引发的DNA双链断裂(DSBs)情况;我们通过CED的方式输送1.1±0.2 MBq 177Lu-AuNPs (4 × 1011 AuNPs)治疗右脑移植U251-Luc肿瘤的NRG小鼠,对照组小鼠给予未标记的aunp或生理盐水,通过单光子发射计算机断层显像/计算机断层扫描(SPECT/CT)成像和生物分布评估177Lu-AuNPs在的肿瘤的摄取情况,以及估算肿瘤、大脑和其他主要器官的辐射剂量;对于治疗效果,我们则通过生物发光成像(BLI)、t2加权磁共振成像(MRI)以及Kaplan-Meier中位生存期,来确定此方法对GBM肿瘤治疗的有效性。治疗14d后通过监测体重、血液学和血液生化分析,以评估正常组织毒性。
通过研究发现177Lu-AuNPs (2.0 MBq, 4 × 1011 AuNPs)可使U251-Luc细胞的克隆存活率降低至0.005±0.002;与未标记的AuNPs或生理盐水处理的细胞相比,DNA DSBs增加14.3倍;NRG小鼠原位U251-Luc肿瘤中177Lu-AuNPs可维持21d的高肿瘤本底比,并且很少通过代谢重新分布到脑或其他器官,且保持高剂量(599 Gy)的肿瘤内放射,而除肿瘤外的正常右脑半球剂量低仅6.4Gy比肿瘤组织剂量低近93倍,此外,对侧左脑半球剂量0.3 Gy、小脑剂量0.2 Gy比肿瘤组织剂量低2000 - 3000倍,外周器官剂量均<0.1 Gy;BLI结果显示,用177Lu-AuNPs处理的小鼠肿瘤生长几乎完全停止,而对照小鼠肿瘤则生长迅;。177Lu-AuNPs治疗后28 d的MRI和组织学染色显示小鼠未见明显肿瘤,而对照组小鼠出现较大的GBM肿瘤,所有对照组小鼠均在治疗后39天(生理盐水)或45天(未标记的AuNPs)内达到近乎人类患者的生命终点,而177 lu -AuNPs处理的小鼠中有5/8存活至150天,且177Lu-AuNPs处理的小鼠未观察到对正常组织的毒性,因此,我们得出结论:177Lu-AuNPs的CED对NRG小鼠脑内U251-Luc人GBM肿瘤非常有效,并且对正常组织无毒。CED给药的177Lu-AuNPs有望治疗GBM患者,并能有效防止复发和改善预后。
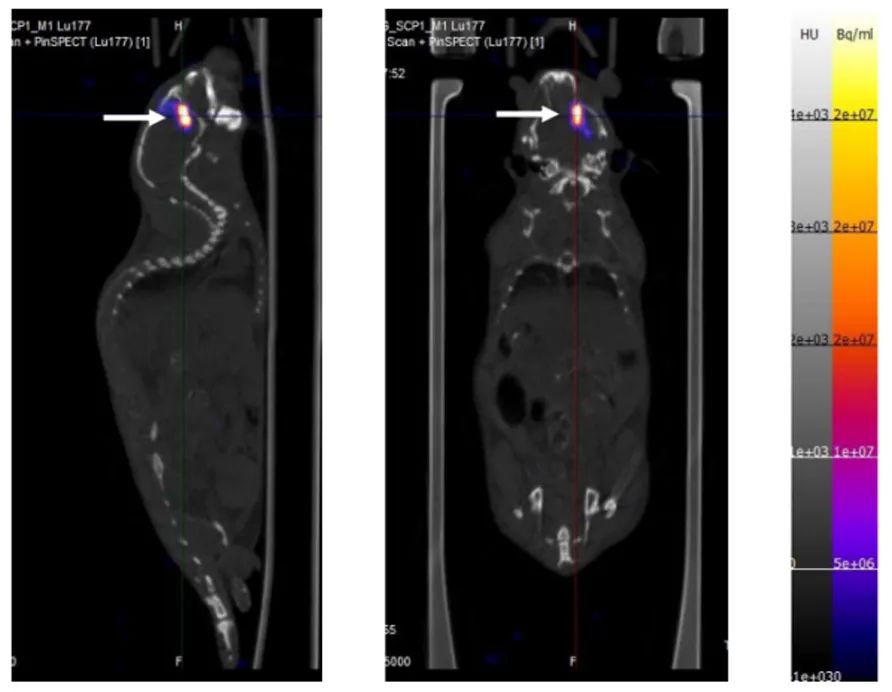
上图在1.0 MBq 177Lu-AuNPs (4 × 1011 AuNPs)治疗14天后,原位U251-Luc人GBM肿瘤NRG小鼠的矢状面(左)和冠状面(右)SPECT/CT全身图像。箭头所示177Lu-AuNPs的活度仅局限于CED输注大脑的部位,没有明显的再分布到身体的其他区域。
研究机构:
Department of Pharmaceutical Sciences, Leslie Dan Faculty of Pharmacy, University of Toronto, 144 College Street, Toronto, OntarioM5S 3M2, Canada
多伦多大学莱斯利·丹药学院药学系
Department of Medical Imaging, Temerty Faculty of Medicine, University of Toronto, Toronto, OntarioM5S 1A8, Canada
多伦多大学Temerty医学院医学影像系
Joint Department of Medical Imaging and Princess Margaret Cancer Centre, University Health Network, Toronto, OntarioM5G 2C1, Canada
医学影像部和玛格丽特公主癌症中心
多伦多大学(University of Toronto,简称UofT,中文简称“多大”)位于加拿大安大略省省会多伦多,是一所公立联邦制大学与研究型大学。
多大医学院及下属的十所世界级研究医院,包括:大学医学网络〔UHN,下含多伦多总医院(Toronto General),玛格丽特公主医院(Princess Margaret),西多伦多医院(Toronto Western)〕,等;构成了加拿大最大的医学及生命科学科研集群。在每年十余亿美元专项科研经费的支持下,其下属的数十间研究机构产生的科研成果无论在数量或质量上都处在世界前十位。