近日,空军军医大学西京医院核医学科汪静教授团队,在国际核医学领域权威期刊《Journal of Nuclear Medicine and Molecular Imaging》上发表了一项突破性病例研究。该研究利用先进的一体化PET/MR设备,首次在活体内、同一位患者身上,直观揭示了帕金森病两大核心病理特征——脑内铁沉积与多巴胺功能障碍——在空间位置上高度重叠,为深入理解该病的发病机制提供了关键的影像学证据。
创新方法:一次扫描,双重观察
帕金森病是一种常见的神经系统退行性疾病,传统认为其核心病理是脑中产生多巴胺的神经元(位于黑质)死亡,导致“多巴胺功能”丧失。近年来,研究也发现患者脑内特定区域(尤其是黑质)存在“铁沉积”异常增多现象。然而,这两种异常变化是各自独立,还是相互关联,一直缺乏直观证据。本研究创新性地使用了可同时进行PET和MR扫描的一体化设备,用¹⁸F-FP-CIT PET显像来精确评估“多巴胺转运蛋白”的功能(即多巴胺能神经元的完整程度),用定量磁敏感成像(QSM)来精确量化脑内“铁含量”。通过同机、同步扫描,确保了两种信息在解剖位置上的精确对应。
关键发现:病理变化的“共定位”现象
研究人员对一位68岁的女性帕金森病患者进行了扫描。结果显示:
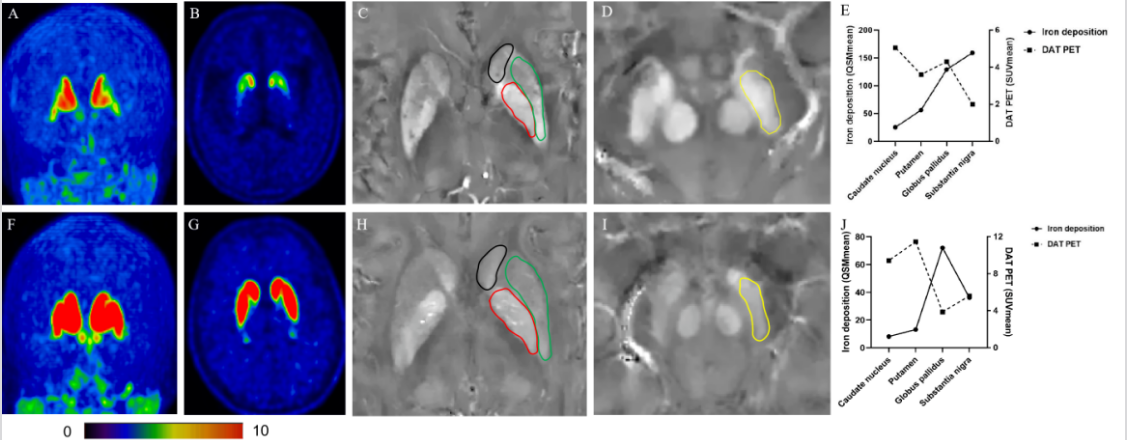
多巴胺功能显著降低:PET图像清晰显示,患者大脑双侧壳核(尤其是后部)及左侧尾状核的多巴胺转运蛋白摄取量显著下降,这是多巴胺神经元受损的直接证据。
铁含量异常升高:QSM图像显示,在患者的黑质致密部、红核、苍白球等核心脑区,铁含量明显高于正常水平。
空间高度重叠:最重要的发现是,铁沉积最严重的脑区(如黑质),恰恰也是多巴胺功能丧失最严重的区域。这种“共定位”现象强烈提示,铁的异常堆积可能与多巴胺神经元的损伤和死亡过程存在协同作用,而非两个独立事件。
科学意义:为“铁死亡”假说提供关键证据
这一发现为帕金森病研究中的前沿理论——“铁死亡”假说提供了有力支持。“铁死亡”是一种铁依赖性的、与脂质过氧化相关的特殊细胞死亡方式。本研究表明,过量的铁可能通过催化氧化应激、促进α-突触核蛋白(帕金森病的特征性病理蛋白)异常聚集等机制,加速了多巴胺神经元的“铁死亡”,从而推动了疾病进展。
临床前景:为诊疗提供新方向
此项研究不仅深化了对帕金森病病理机制的理解,更具有重要的临床转化潜力。它提示,未来针对帕金森病的治疗,除了补充多巴胺,调控脑内铁代谢、使用铁螯合剂或抗氧化药物来保护神经元,可能成为新的神经保护治疗策略。同时,一体化PET/MR这种多模态成像技术,有望成为评估疾病进展、筛选潜在治疗患者和监测新药疗效的强大工具,推动帕金森病的精准诊疗。