国际核药研发领域取得重要进展。近日,期刊《npj Imaging》上发表了一项研究,成功开发了一种名为rhTATE4的新型放射性杂合分子,旨在解决神经内分泌肿瘤诊疗中诊断与治疗药物不匹配的长期难题。
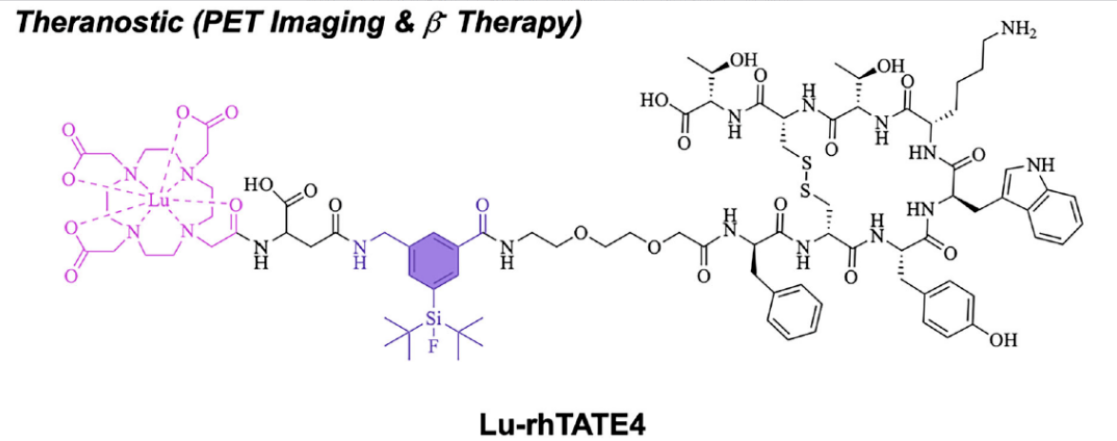
目前临床标准方案中,用于PET成像的⁶⁸Ga-DOTA-TATE与用于治疗的¹⁷⁷Lu-DOTA-TATE因核心金属离子(Ga³⁺与Lu³⁺)不同,导致两种药物在体内的代谢行为存在差异,使得诊断影像无法精确预测治疗效果。rhTATE4采用了创新的“放射性杂合”设计策略,在同一分子骨架上整合了两个独立的核素结合位点,可分别标记¹⁸F用于PET成像,或标记¹⁷⁷Lu用于β⁻射线治疗,从而实现了诊断版与治疗版药物的化学结构完全相同,确保了其体内行为的高度一致性。
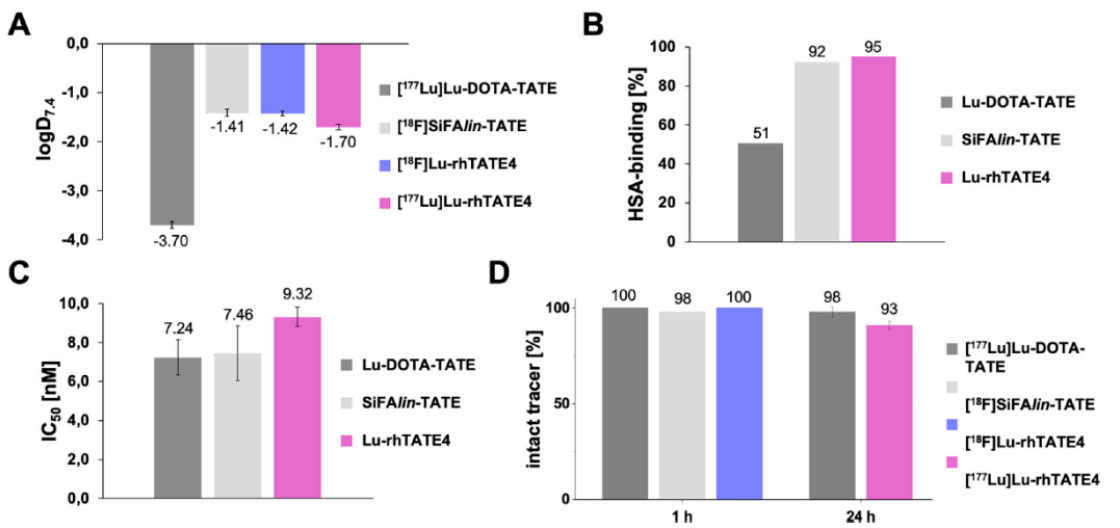
在临床前研究中,该分子展现出卓越的综合性能。体外实验表明,其受体亲和力与血浆稳定性与现有临床金标准药物相当。在荷瘤小鼠模型中,其诊断版本¹⁸F-rhTATE4表现出创纪录的高肿瘤摄取,达到53.58% ID/g,约为当前基准药物的3倍,且肿瘤与背景对比鲜明。其治疗版本¹⁷⁷Lu-rhTATE4在肿瘤中的24小时滞留率(10.32% ID/g)与金标准药物相当,关键在于显著降低了在肺、胰腺、肾上腺、肾脏等正常器官中的非特异性蓄积,意味着其潜在的治疗窗口更大,对正常组织的损伤风险更低。此前类似设计的分子曾因肾脏摄取过高而无法用于治疗,本研究通过引入新型亲水性模块成功解决了这一瓶颈。
该研究的成功标志着放射性杂合药物开发在sstR2靶点上的重大突破。rhTATE4是首个在该靶点上同时实现超高肿瘤摄取和更低正常器官蓄积的一体化诊疗分子。这一设计范式不仅有望推动神经内分泌肿瘤诊疗的精准化,也为针对其他肿瘤靶点的放射性杂合诊疗药物开发提供了可借鉴的通用平台,具有重要的临床转化潜力。