
近日,智核生物宣布,其自主研发的68Ga标记PD-L1的放射性显影剂药物(SNA002),已获得了美国食品药品监督管理局(后简称“FDA”)的新药临床试验(后简称“IND”)批准,可正式进入临床试验阶段。SNA002是一款以单域抗体为前体的,偶联放射性PD-L1表达的PET显影药物,拟用于评估实体瘤患者原发和/或转移病灶PD-L1表达水平。
此次SNA002在美国FDA获得临床试验批准,对整个核药行业来讲具有里程碑式意义——标志着中国创新核药企业正式开发出放射性核素药物向美国FDA递交IND申请的完整路径,中国创新核药的研发开始与国际接轨,这将极大地鼓舞核药领域的相关企业。SNA002将有望成为中国首个登陆欧美的新型核素药物。
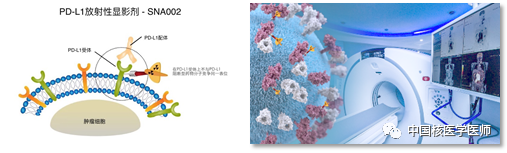
SNA002是68Ga标记PD-L1的放射性显影剂,注射后1-2小时内即可通过PET-CT的方式进行显影,实时、动态显示全身各脏器PD-L1表达水平,包括肿瘤内部和微小转移灶的异质表达,可实现:
Ø 精准筛选出对PD-1治疗有效的人群,指导肿瘤患者精准用药,符合伦理、提升患者生活品质、节约患者医疗费用和国家医保资金;
Ø 打破了有创式取样进行免疫组化的传统检测方式,减轻患者痛苦的同时,能够根据疾病发展情况随时进行显影检查。
如今PD-(L)1单抗已经成为全球最成熟的产品,据Frost &Sullivan 数据显示,到2023年,全球PD-(L)1抑制剂市场将达639亿美元。而在中国,预计2023年市场规模将达664亿元人民币。PD-L1检测在免疫检查点抑制剂疗效预测的可及性和循证医学证据等方面发挥着非常重要的作用。基于此PD-L1 检测已经写进了肺癌 NCCN 指南和 CSCO 指南,但由于PD-L1的表达具有时空异质性,传统的免疫组化检测方式如单个部位及单次取样、局部取样等缺点不能准确反应全身 PD-L1 表达情况,使用SNA002进行PET-CT显影可以规避免疫组化方式的缺陷。
智核生物创始人须涛表示:我们获得了第一个出海的68Ga单域抗体放射性药物FDA的IND批准,证明智核已经打通了放射性药物特别是基于单域抗体为前体的分子发现、验证、工艺开发、注册等链条,后续项目将批量化产出。当然这只是万里长征第一步,希望接下来能够以最快的速度将产品从临床前阶段推至临床阶段最终到商业化推广阶段。我们也希望国内的创新核药企业能够在国家政策利好的情况下厚积薄发,尽快达到与欧美核药领域媲美的水平。