随着核技术的广泛使用,如何对电离辐射引起的急性损伤进行有效防护已经成为一项重要研究课题。当电离辐射作用于机体时,会产生大量活性氧自由基,可以破坏细胞内的关键组分,如脂质、蛋白、RNA和DNA等,引起细胞、组织损伤甚至机体死亡。目前,常见的辐射防护剂主要为小分子药物,普遍存在水溶性差、毒副作用严重和生物半衰期短等缺陷,从而限制了它们在临床中的进一步应用。因此,研发安全、高效的辐射防护药物,对降低核突发事件及医疗中的辐射危害具有重要意义。
针对小分子辐射防护剂存在的问题,苏州大学华道本教授团队报道了一种含硒高分子药物应用于高效辐射防护的新策略。该团队前期研究发现,高分子纳米药物载体能明显改善小分子药物的水溶性和生物相容性,延长其血浆半衰期并增强作用效果。因此,通过活性自由基可控聚合,将乙烯基苯基硒醚(VSe)和N-(2-羟乙基)丙烯酰胺(HEA)进行共聚,制备了两亲性含硒高分子药物可直接用于辐射防护(图1)。其中疏水性的硒醚基团可清除活性氧自由基,发挥辐射防护作用,同时被氧化为亲水性的硒亚砜或硒砜。与小分子辐射防护剂相比,该高分子药物毒性低,血液内循环时间长,单次给药即可高效辐射防护。
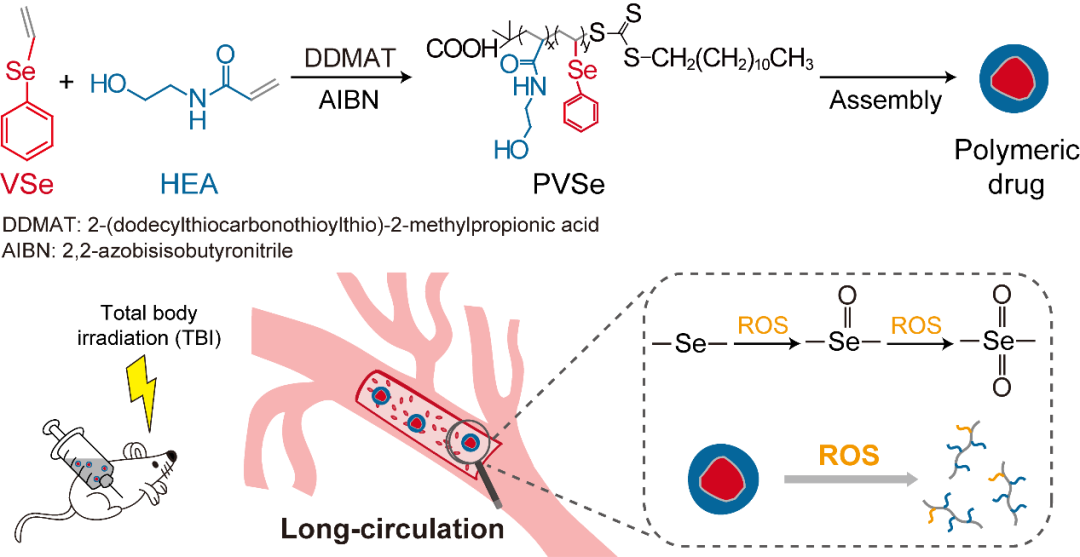
图1:高分子药物的合成路线及放射防护原理图。(Copyright 2020, American Chemical Society)
该工作通过单次用药进行了动物体内辐射防护研究(图2)。对C57BL/6小鼠进行8 Gy全身辐照前,同样硒浓度的高分子药物和商业化的小分子药物依布硒相比,高分子药物可提高动物的照后生存率至30%,同时有效缓解急性辐射引起造血系统损伤,而该剂量下依布硒无明显辐射防护效果。小鼠接受8 Gy全身照射后第7天,高分子药物可减轻急性辐射引起的外周血细胞数量下降程度;照射后第30天,高分子药物处理组小鼠的外周血红细胞和血小板数量可基本恢复至对照组小鼠水平。单次给药即可达到有效辐射防护效果能够大大提高给药的便利性及患者的顺应性,为高分子药物的进一步应用奠定了基础。
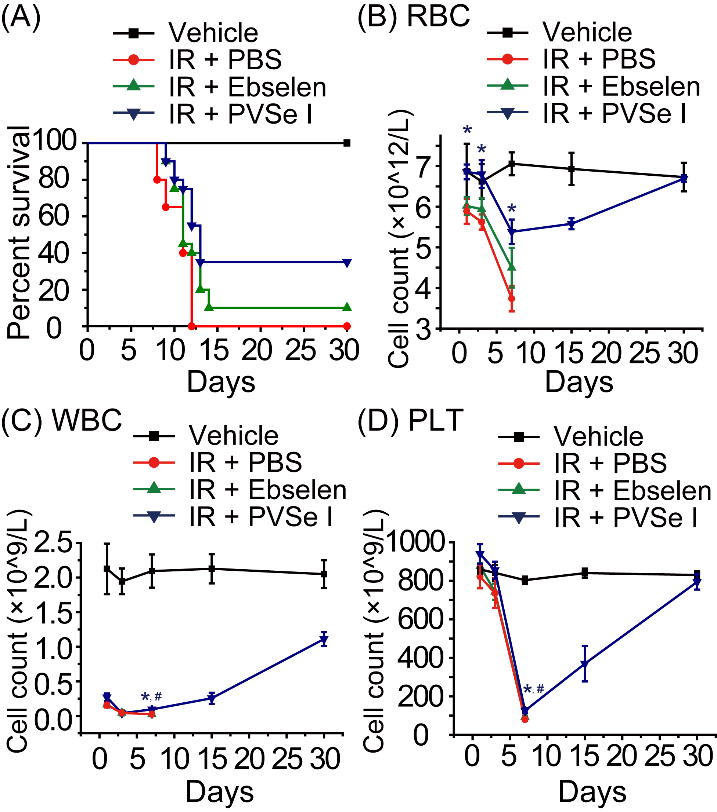
图2:(A)8 Gy全身照射后小鼠30天存活率;照射后不同时间点小鼠外周血(B)红细胞,(C)白细胞和(D)血小板数量变化。(Copyright 2020, American Chemical Society)
同时对高分子药物的药代动力学进行了分析(图3)。发现其血浆清除半衰期可达10小时,明显优于商业化小分子药物依布硒(3小时)。高分子药物中的HEA部分具有抵抗非特异性蛋白吸收的能力,且药物本身表现为中性表面电荷,因此可有效延缓高分子药物被网状内皮吸收从而延长其半衰期。高分子药物在小鼠主要器官中保留时间可达72小时,可以起到长效辐射防护作用。另外,研究发现高分子药物在接受8 Gy全身辐照后的小鼠体内半衰期缩短至7小时。这是由于两亲性的含硒醚高分子药物清除ROS之后被氧化为亲水性的含硒亚砜高分子或含硒砜高分子,药物的水溶性增加导致半衰期缩短和代谢速度加快,这种现象可能有效提升高分子药物的生物安全性。
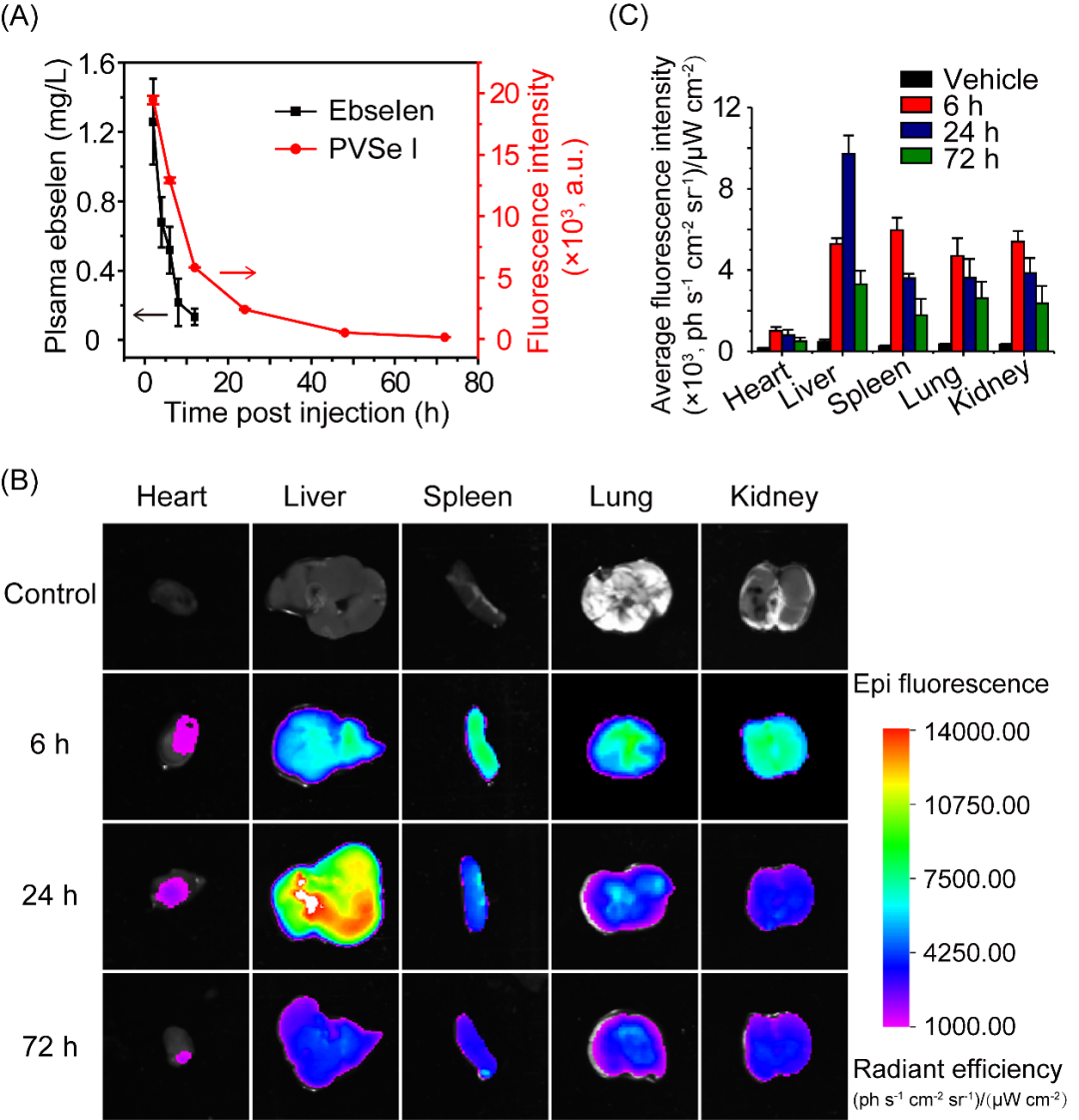
图3:(A)高分子药物和依布硒的血浆清除半衰期;cy5.5荧光标记的高分子药物在小鼠不同器官的(B)体外荧光图像及(C)荧光强度定量结果。(Copyright 2020, American Chemical Society)
该论文的第一作者为苏州大学放射医学与辐射防护国家重点实验室的博士生王璐,通讯作者为华道本教授,相关成果以“Strategy for Highly Efficient Radioprotection by a Selenium-Containing Polymeric Drug with Low Toxicity and Long Circulation”为题发表在ACS Applied Materials & Interfaces, 2020, DOI:10.1021/acsami.0c14000。





