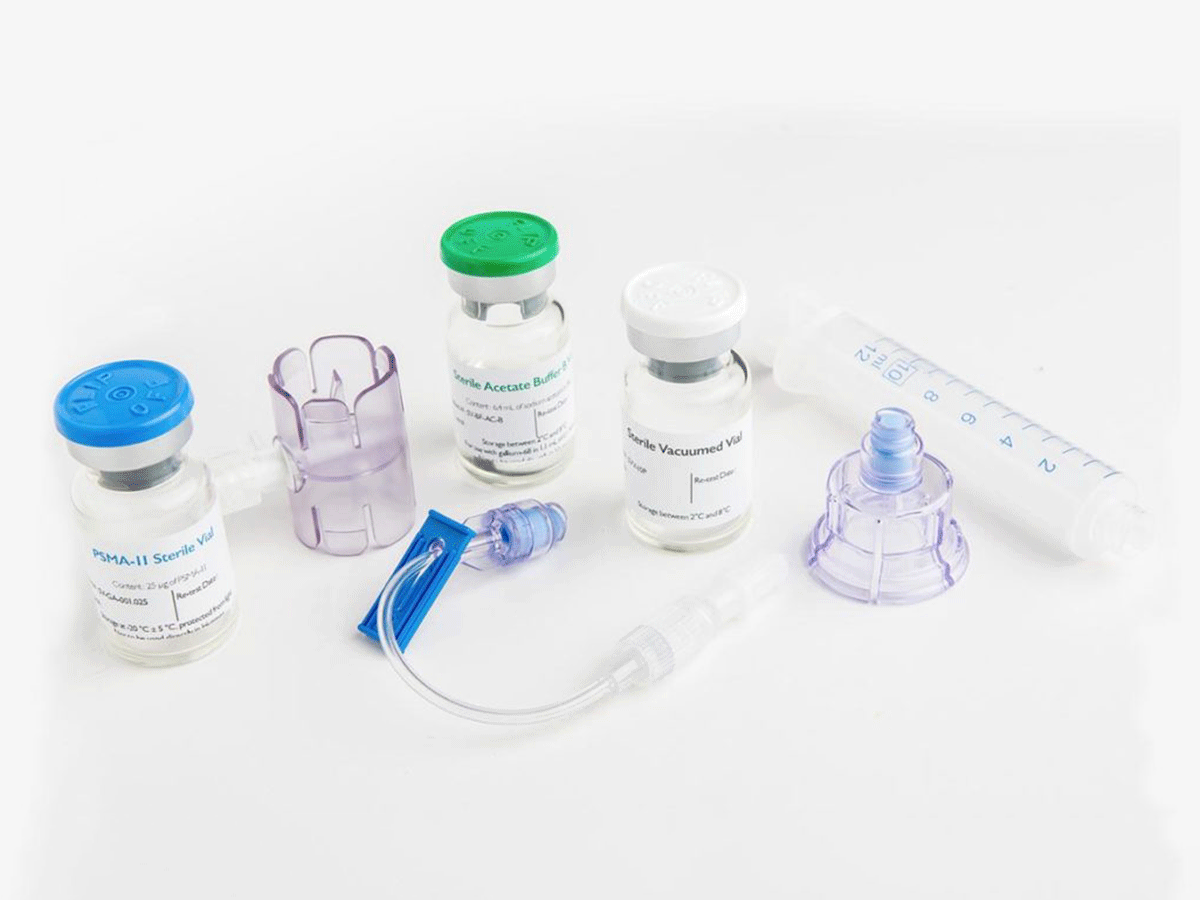
2021年3月8日,香港——远大医药(00512.HK)欣然宣布,集团联营公司Sirtex Medical Pty ltd (「Sirtex」) 重磅抗肿瘤药物SIR-Spheres® 钇[90Y]树脂微球近期获得英国国家健康照护专业组织(「NICE」)推荐用于治疗不可切除的晚期肝细胞癌(HCC)成人患者;以及获得美国食品药品管理局(「FDA」)批准开展原发性肝癌(HCC)临床试验。

SIR-Spheres® 钇[90Y]树脂微球为一款针对肝脏恶性肿瘤的靶向内放射核素产品,采用全球领先的介入技术将SIR-Spheres® 钇[90Y]树脂微球注入肝脏肿瘤血管,释放高能量β放射线杀灭肿瘤细胞,是目前全球唯一获得FDA正式批准的放射性微球。
NICE为英国国家卫生服务机构重要组织,也是全球公认顶级卫生技术评估机构之一,全球75%以上的政府和卫生技术评估机构都将NICE的推荐意见作为将产品纳入本国医保报销的重要决策依据。根据NICE推荐,在英格兰和威尔士,对于Child-Pugh A级肝功能、不适合传统经动脉疗法的HCC成人患者,使用SIR-Spheres® 钇[90Y]树脂微球进行选择性内放射治疗(SIRT)将给予全额资助和报销,预计每年在英国将增加近千名患者使用SIR-Spheres® 钇[90Y]树脂微球进行治疗。此外, NICE的推荐对SIR-Spheres® 钇[90Y]树脂微球的全球医保报销准入也具有里程碑式的意义,有望加速其在其他新兴市场(如巴西)医保报销的准入,进一步拓展其市场份额,帮助全球范围内更多肝癌患者接受SIR-Spheres® 钇[90Y]树脂微球治疗。
另外,本次SIR-Spheres® 钇[90Y]树脂微球获FDA批准开展原发性肝癌(HCC)临床试验,以在美国申请原发性肝癌的上市许可。该临床试验为单臂临床试验,将于近期进行病人入组。
临床研究证实,SIR-Spheres® 钇[90Y]树脂微球可显著提高肿瘤反应率,使患者肿瘤缩小、降期并重获肝切除术机会;并显著延长肝脏无进展生存期,控制患者肝脏肿瘤进展,增加等待肝移植手术的时间;同时,副作用较小、患者生活质量较高。凭借其显著的临床疗效,SIR-Spheres® 钇[90Y]树脂微球已在全球超过50个国家和地区累计治疗超过10万人次,获得美国国立综合癌症网络(「NCCN」)、欧洲肿瘤内科学会指南(「ESMO」)等多个权威指南推荐用于治疗肝脏恶性肿瘤;纳入美国及欧洲等多地医保;并分别进入2019版的中国「原发性肝癌诊疗规范」和2018版「中国结直肠癌肝转移诊断和综合治疗指南」。
董事会表示:“近期两项重大进展证明SIR-Spheres® 钇[90Y]树脂微球的临床疗效和竞争优势,有助于帮助全球范围内更多肝癌患者接受治疗。”本次获得NICE推荐,证明了SIR-Spheres® 钇[90Y]树脂微球的治疗对HCC患者生活质量和经济效益具有积极影响。
未来集团将持续布局抗肿瘤领域,以患者需求为核心,以科技创新为驱动,加大对放射性药物和免疫抗肿瘤全球创新产品的投入,并联合美国的OncoSec、澳洲的Sirtex和Telix Pharmaceuticals Limited (ASX: TLX)三家全球领先的抗肿瘤医药公司,针对尚未满足的临床需求,持续开发不同癌种的全球创新产品,丰富和完善产品管线及产业布局,打造国际领先的放射性药物和免疫抗肿瘤平台;采用「全球化运营布局,双循环经营发展」策略,形成国内国际双循环联动发展并相互促进的新格局,充分发挥本集团在国内的产业优势和研发实力,快速将国际创新产品落地,为全球肿瘤患者提供更先进更多样的治疗方案。”



![拜耳氯化镭[223Ra]注射液中国获批用于前列腺癌治疗](https://www.ccnta.cn/uploadfile/2020/0903/20200903091221792.png)