动脉粥样硬化是心肌梗死、脑卒中等致死性心血管事件的主要病理基础,其临床诊断的核心难题在于:传统影像(如CT、超声)难以在急性事件发生前,无创地准确识别斑块的存在,更无法评估其易损性。针对这一未被满足的临床需求,能够靶向特定生物学过程(如炎症、脂质积聚)的核医学分子影像技术(如PET/CT)展现出独特优势。然而,常规PET示踪剂存在靶向特异性不足等局限,这催生了将纳米脂质体作为智能递送载体的创新策略。纳米脂质体具有可生物降解、低毒性、易于表面功能化修饰、可延长体内循环时间等优点,有望将放射性核素精准递送至斑块部位,实现高对比度的分子显像。
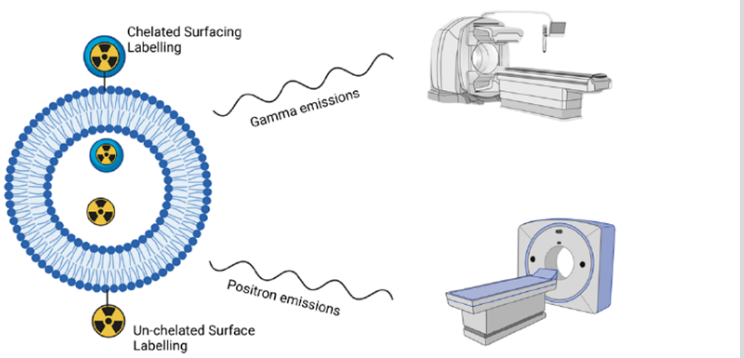
构建用于斑块显像的纳米脂质体放射性药物涉及三大核心环节。首先,是放射性核素标记。可通过将核素(如用于PET的⁶⁴Cu、⁸⁹Zr)整合到脂质体膜表面,或包裹在其内部水核中来实现。其次,是优化体内行为。通过表面修饰聚乙二醇(PEG)等亲水性物质,可有效减少被肝脏、脾脏等单核吞噬系统快速清除,从而延长血液循环时间,增加其在斑块区域的被动蓄积(即增强渗透与滞留效应)。最后,是实现主动靶向。通过在脂质体表面连接特异性抗体、多肽等功能分子,可使其主动识别并结合斑块内过度表达的炎症细胞、黏附分子或细胞外基质成分,极大提升显像的特异性和灵敏度。
临床前研究已为该技术提供了有力证据。例如,在动脉粥样硬化动物模型中,⁸⁹Zr标记的PEG化脂质体可在血管壁病变处出现显著摄取;¹¹¹In标记的特定磷脂脂质体可被斑块内的巨噬细胞有效吞噬,从而可视化斑块。这些研究证实了基于脂质体的PET探针在早期检测、风险分层和治疗监测方面的潜力。然而,其临床转化仍面临关键挑战,包括需要深入阐明纳米粒与人体生物系统的复杂相互作用、系统评估其生物安全性与免疫原性,并优化粒径、表面性质等参数。未来,该领域将向多模态成像(如整合PET、MRI、荧光)和诊疗一体化(即同一载体兼具诊断与治疗功能)方向发展,旨在为动脉粥样硬化的精准管理与个体化治疗提供革命性工具。