中国医学科学院放射医学研究所刘鉴峰研究员团队在放疗联合免疫治疗领域取得重要突破。
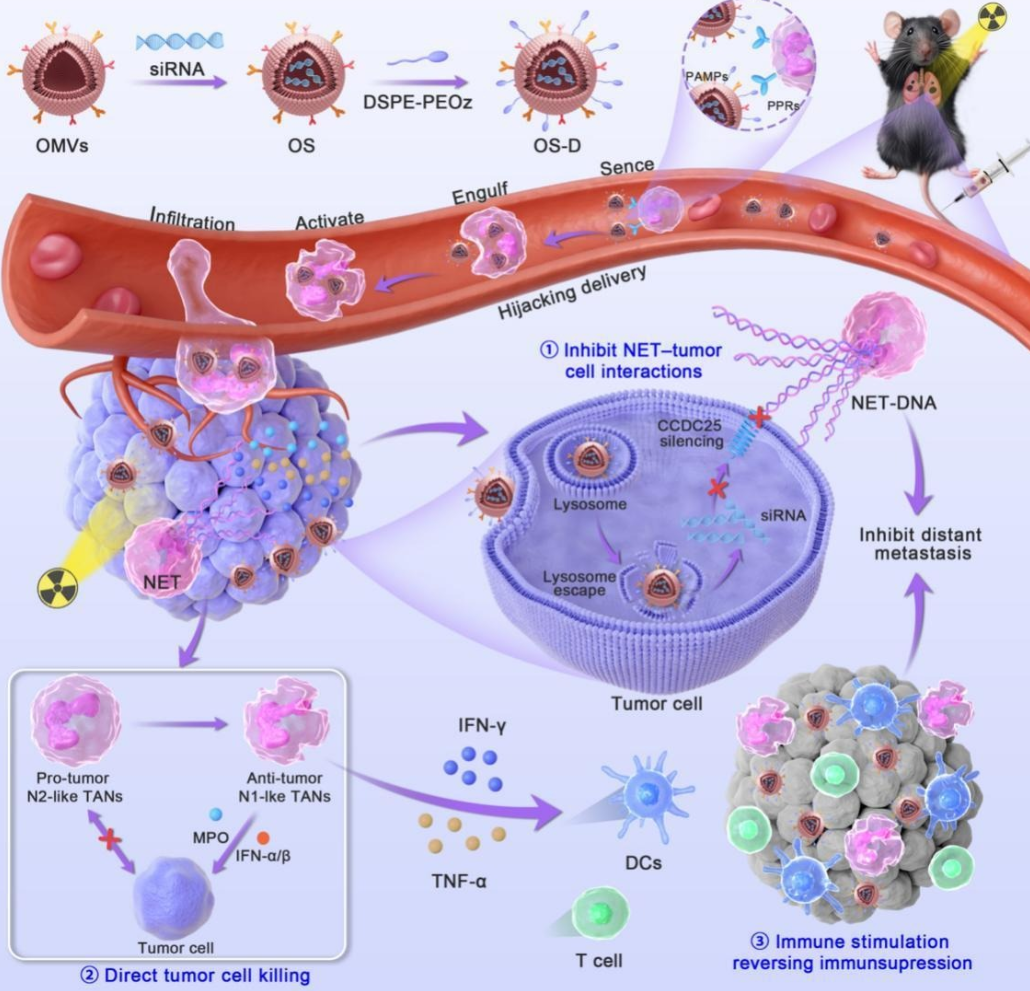
针对放疗在杀伤肿瘤的同时可能诱导炎症、招募中性粒细胞并形成中性粒细胞胞外陷阱(NETs)进而促进肿瘤远处转移的临床难题,研究团队成功构建了一种“劫持”中性粒细胞的多功能纳米平台(OS-D),将靶向CCDC25的siRNA装载进来源于大肠杆菌外膜囊泡的载体中,并用pH敏感材料进一步修饰,使其能够在肿瘤微环境中更有效地释放药物。
研究指出,放疗虽能杀伤肿瘤细胞,但也会诱发炎症反应,招募大量中性粒细胞,并促进中性粒细胞胞外诱捕网(NETs)形成。这些NETs会被肿瘤细胞表面的DNA感受器CCDC25识别,进而触发细胞骨架重塑和迁移信号,增加肿瘤扩散和远处转移风险。
OS-D的设计思路是借助放疗后中性粒细胞向肿瘤聚集的过程,实现更精准的递送。外膜囊泡富含病原相关分子模式,能够被中性粒细胞优先吞噬,并随其迁移进入肿瘤部位。到达炎症性肿瘤微环境后,OS-D释放siRNA,沉默肿瘤细胞中的CCDC25,从而切断NETs促进转移的关键信号通路。
除了递送基因沉默药物,OS-D还可促使中性粒细胞向抗肿瘤表型转变。研究显示,这类被重新编程的中性粒细胞能够分泌更多具有细胞毒性和免疫刺激作用的因子,增强抗肿瘤免疫反应,并有助于逆转肿瘤微环境中的免疫抑制状态。
研究团队认为,这一策略把免疫调节与基因沉默结合起来,不仅提升了放疗效果,也为抑制放疗诱导的肿瘤进展和转移提供了新的思路。由于所用外膜囊泡来源于无致病性、且对常用抗生素敏感的大肠杆菌菌株,该平台也显示出一定的安全性和临床转化潜力。