放射性药物治疗(RPT)已彻底告别“最后选择”的边缘地位,凭借²²³RaCl₂、¹⁷⁷Lu-DOTATATE和¹⁷⁷Lu-PSMA-617在关键III期试验中的成功,成为肿瘤精准治疗的标准选项之一。截至2024年9月,全球共有34项活跃的III期临床试验,标志着该领域进入循证证据快速积累期。从适应症分布看,神经内分泌肿瘤和前列腺癌是当前研究的绝对核心,合计占比近四分之三。在核素选择上,¹⁷⁷Lu因其平衡的物理特性(半衰期6.7天、适中的β能量、可显像)成为主导,在17项研究中被使用;同时,α核素(如²²⁵Ac、²²³Ra)因更高的线性能量传递和更短射程,在克服耐药方面展现出巨大潜力,正获得越来越多的关注。
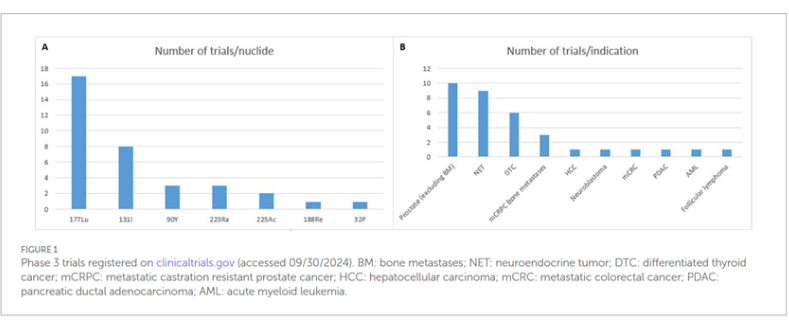
在各癌种中,RPT研究呈现出显著的“前移”与“扩展”趋势。在神经内分泌肿瘤领域,研究正从已获批的G1/G2级胃肠胰神经内分泌肿瘤,向更高分级(G3)及一线治疗推进,例如NETTER-2研究已提示¹⁷⁷Lu-DOTATATE可作为G2/G3患者的一线新标准。在前列腺癌领域,PSMA靶向治疗是爆发点,多项大型III期试验(如PSMAfore、PSMA-addition、规模巨大的STAMPEDE2)正推动¹⁷⁷Lu-PSMA-617的适应症从晚期去势抵抗阶段,前移至转移性激素敏感期甚至寡转移阶段。此外,在甲状腺癌、肝细胞癌、血液肿瘤等领域也有重要研究进行,例如探索在低危甲状腺癌中避免放射性碘治疗,或评估新型放射免疫药物在急性髓系白血病中的作用。
当前RPT的发展核心聚焦于四大方向:一是适应症不断前移和扩展;二是推动剂量个体化,即基于诊断性显像(如⁶⁸Ga-PSMA PET)的药代动力学来制定治疗剂量,取代固定剂量方案;三是深入探索联合治疗策略,与化疗、靶向治疗、免疫治疗等协同;四是深化诊疗一体化理念,实现诊断与治疗配体的精准配对。然而,该领域仍面临一系列关键挑战,包括如何优化患者筛选、确定最佳剂量与周期、解析耐药机制以及优化与其他疗法的联合时序。正在进行的众多III期研究,有望为这些问题的解决提供高级别证据,进一步巩固RPT在肿瘤综合治疗版图中的核心地位。