2026年4月13日,国际权威核医学期刊《European Journal of Nuclear Medicine and Molecular Imaging》(中科院1区/Q1,IF=7.6)在线发表了新加坡国立大学、 厦门大学、山东肿瘤医院核医学与分子成像中心 等研究团队题为《Enhanced therapeutic efficacy of sequential ¹⁷⁷Lu/²²⁵Ac-LNC1004 FAP-targeted radionuclide therapy combined with anti-PD-L1 blockade in pancreatic cancer》的研究成果。

该研究针对胰腺癌“冷肿瘤”免疫抑制微环境,创新性地采用成纤维细胞活化蛋白(FAP)靶向放射性核素治疗(TRT) 联合免疫检查点抑制剂,在 Panc02 胰腺癌小鼠模型中实现了肿瘤完全消退 。
作者团队: Mengqi Shi, Jia Liu, Heng Li, Sze Chun Leo Chan, Yinghao Cao, Xueyuan Zeng, Yongliang Zhang, Zhide Guo, Xuejun Wen (通讯作者), Jingjing Zhang (通讯作者), Xiaoyuan Chen (通讯作者)。
引用格式: Shi M, Liu J, Li H, et al. Enhanced therapeutic efficacy of sequential ¹⁷⁷Lu/²²⁵Ac-LNC1004 FAP-targeted radionuclide therapy combined with anti-PD-L1 blockade in pancreatic cancer. Eur J Nucl Med Mol Imaging. 2026. https://doi.org/10.1007/s00259-026-07878-3
胰腺导管腺癌恶性程度极高、预后极差,5 年生存率仅约 13%,其核心治疗瓶颈在于:致密的肿瘤微环境(TME) 富含表达成纤维细胞活化蛋白(FAP) 的癌相关成纤维细胞(CAFs),形成物理屏障并抑制免疫浸润;属于典型免疫 “冷肿瘤”,PD‑1/PD‑L1 抑制剂单药几乎无效;传统放化疗、靶向治疗疗效有限,亟需突破免疫抑制与基质屏障的新方案。
FAP 作为胰腺癌基质的关键靶点,靶向核素治疗(TRT)既可杀伤 CAFs、重塑微环境,又可通过辐射诱导免疫原性细胞死亡,为免疫治疗创造 “窗口期”。
本研究创新性将β 核素 ¹⁷⁷Lu与α 核素 ²²⁵Ac标记的长效 FAP 抑制剂 LNC1004,与 PD‑L1 抑制剂序贯联用,探索协同增效机制与最优方案。
本研究采用的核素探针包括¹⁷⁷Lu‑LNC1004(β 射线,兼具显像与治疗)、²²⁵Ac‑LNC1004(α 射线,高 LET 强效杀伤);动物模型选用免疫健全 C57BL/6 小鼠皮下接种 Panc02 胰腺癌细胞;治疗分组设置了对照组、PD‑L1 单抗单药、不同剂量 ¹⁷⁷Lu‑LNC1004 单药、²²⁵Ac‑LNC1004 单药,以及核素治疗后 4 小时序贯给予 PD‑L1 抑制剂的联合组;评估指标涵盖 SPECT/CT 显像、体内分布、肿瘤生长曲线、生存期、免疫微环境流式分析、组织病理等。
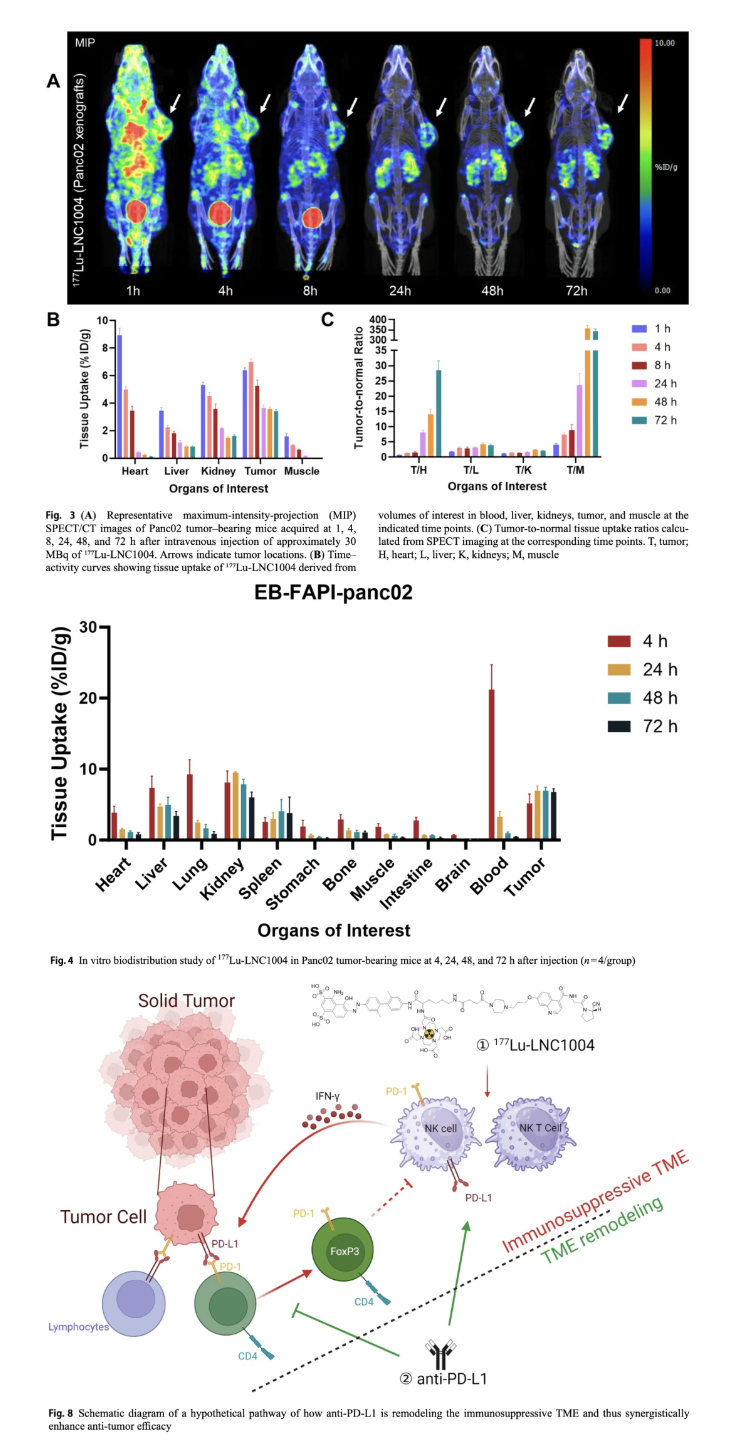
研究核心结果显示,¹⁷⁷Lu‑LNC1004 在胰腺癌中呈高摄取、长滞留,SPECT/CT 与离体分布显示,注射后 1 小时肿瘤即显影,72 小时仍保持高摄取,且正常组织清除快,肿瘤 / 本底比持续升高,72 小时肿瘤 / 血比达15.37,为精准治疗奠定基础。
在β 核素联合免疫方面,30 MBq ¹⁷⁷Lu‑LNC1004+PD‑L1 抑制剂实现肿瘤完全消退,其中单药 PD‑L1、低 / 中剂量 ¹⁷⁷Lu‑LNC1004 仅部分抑制肿瘤,而30 MBq ¹⁷⁷Lu‑LNC1004 序贯 PD‑L1 抑制剂组在40 天观察期内所有小鼠肿瘤完全消失,无复发,且体重无明显下降,肝肾无明显病理损伤,安全性良好。
α 核素联合免疫则表现为极低剂量 ²²⁵Ac‑LNC1004 即实现强效持久应答,仅37 kBq ²²⁵Ac‑LNC1004联合 PD‑L1 抑制剂,在90 天随访期内,6/8 小鼠肿瘤完全清除,显著延长生存期,疗效优于 β 核素联合方案,展现 α 核素在实体瘤中的巨大潜力。
协同机制方面,¹⁷⁷Lu‑LNC1004 可杀伤 FAP⁺ CAFs,破坏基质屏障,辐射上调肿瘤微环境PD‑L1⁺免疫细胞,激活 IFN‑γ⁺效应 T 细胞、NK 细胞与 NKT 细胞,序贯 PD‑L1 抑制剂逆转 Treg 介导的免疫抑制,将辐射诱导的 “免疫激活窗口” 转化为持久抗肿瘤免疫,实现 1+1>2 的协同效果。
该研究首次在同源胰腺癌模型证实 FAP 靶向核素治疗 + PD‑L1 抑制剂可完全清除肿瘤,突破胰腺癌免疫治疗耐药;通过β/α 核素双路径验证,明确¹⁷⁷Lu 适合大病灶减瘤与显像指导,²²⁵Ac 适合微小病灶与耐药克隆清除,为序贯双核素联合免疫提供理论依据;同时支持FAP 核素诊疗一体化进入胰腺癌临床探索,尤其针对晚期、转移性、常规治疗失败患者。