有一种癌症,经过30年不懈的努力,正在成功地由“绝症”转变为“慢性病”。毫无疑问,这就是乳腺癌。在2021年2月4日的世界癌症日,一则“乳腺癌已成为全球最常见癌症”登上微博热搜,引发了网友们的热议。
世卫组织癌症专家安德烈 · 伊尔巴维表示,2020年确诊癌症的患者高达1930万人,其中1000万人死于癌症。目前全球有20%的患者在其一生中会罹患癌症。乳腺癌在新增癌症病例中占11.7%,其次是肺癌、结直肠癌。 幸运的是,乳腺癌已不再是“绝症”,已逐步向“慢性病”的方向转变。 根据2019中国临床肿瘤学会(CSCO)乳腺癌年会上获悉的资料显示, 我国乳腺癌患者5年生存率已达83.2%,比过去10年间提高了7.3%。
就在2019年10月18日,第十四届上海国际乳腺癌论坛上发表的一项研究中显示,乳腺癌已经从绝症变成慢性病。这项研究中选取的是20085例进行乳腺癌手术的乳腺癌患者,0期~III期5年无病生存率为85.5%,乳腺癌原位癌5年总生存率高达97.9%,II期和III期患者5年平均生存率分别为75%和61%。未来5年,医院乳腺癌患者5年生存率还能有望提高3%~5%!
乳腺癌不可怕,最可怕的是复发
通常来讲,乳腺癌经过规范的治疗后,患者的生活也会逐渐走向正常化。但是,乳腺癌的复发问题却让患者很担忧。有数据表示,在行乳腺癌手术后1~3年里,60%~80%的患者会复发,而在这些复发的患者里面,又有1/4的患者会死亡。因此,很多人对于乳腺癌复发的恐惧很大。
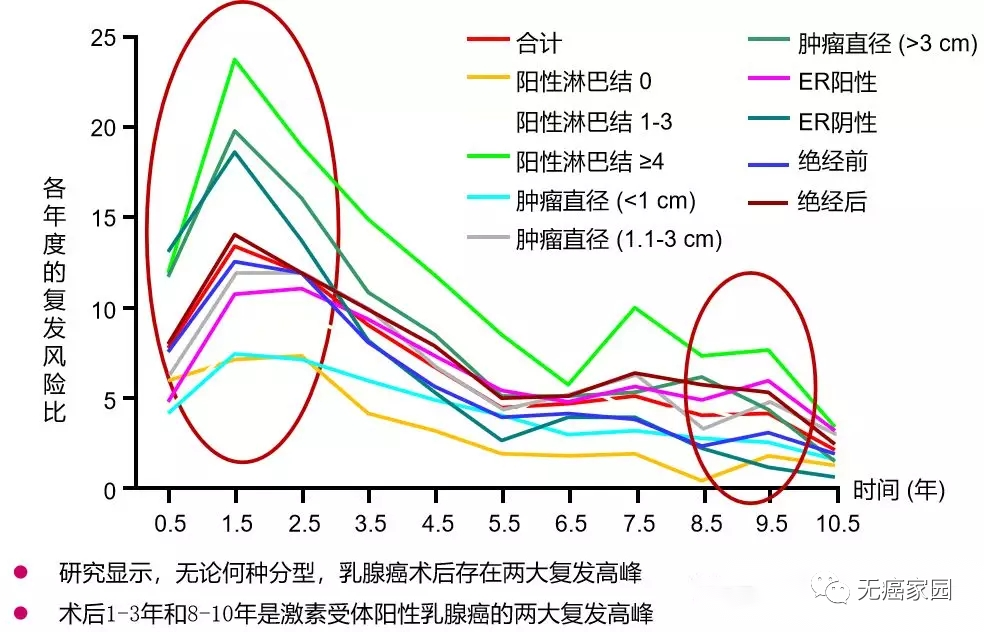
但是又有很多乳腺癌患者认为,手术做完后肿瘤也切掉了,该做的化疗也都做了,是否算是治好了呢?在这里,小编要提醒各位癌友,无论何种分型,乳腺癌术后存在两大复发高峰。术后1~3年和8~10年是激素受体阳性乳腺癌的两大复发高峰。因此,患者进行康复治疗不仅仅是术后的3~5年,更应该是5~10年甚至更长时间。对待乳腺癌,应该做到积极地预防复发,即使局部或区域复发,只要规范辅助治疗仍有治愈的可能;而肿瘤一旦发生远处转移,治愈虽然很难,但若积极治疗,仍能够延长生存期。
预防复发,合理应用辅助治疗
目前,术前进行新辅助治疗,术后进行规范的辅助治疗(化疗、放疗、内分泌治疗及靶向治疗等),均能最大限度降低乳腺癌的复发转移风险。
01 新辅助治疗
新辅助治疗是指主要治疗手段(比如手术)之前做的一种治疗(包括新辅助化疗、新辅助靶向治疗、新辅助内分泌治疗等),是从乳腺癌引入的一个相关性概念。其目的在于:
使肿瘤缩小,杀灭看不见的转移细胞,提高整体治疗效果
降低肿瘤临床分期,提高切除率和保乳率
让本来需要全切的患者保住器官,例如全切的乳腺癌转为可保乳的情况
了解患者肿瘤对什么药物敏感
新辅助化疗适应证,满足其一即可:
1. 肿瘤比较大,直径超过5cm;
2. 腋窝淋巴结已有转移
3. HER-2高表达
4. 三阴乳腺癌患者有保乳想法,但由于肿瘤和乳房比例问题无法保乳的。
02 术后辅助放疗
有临床研究表明,乳腺癌根治术后实施辅助放疗,5年局部率下降17%,15年乳腺癌相关死亡率下降5.4%。因此,采取早期乳腺癌保乳术后的根治性放疗,是保乳治疗不可缺少的部分。 Ⅰ、Ⅱ期患者选择性乳房切除术后胸壁和区域淋巴结的术后放疗,可有效降低局部复发率,并在一定程度上提高生存率。此外,术后辅助放疗也是局部晚期患者综合治疗的必需手段之一;局部区域性复发患者的放射治疗,是重要的补救性治疗措施;转移性患者的姑息性放疗,如骨转移患者的止痛、预防病理性骨折、脑转移患者降低颅内压等,可改善患者在带瘤生存期间的生存质量,并延长部分患者的生存时间。
质子治疗对乳腺癌的益处
1. 高能、精确瞄准的质子束可以提供高剂量的辐射来破坏癌细胞,从而降低多种癌症的复发率。 2. 质子治疗是非侵入性的,可以减少副作用。 3. 接受质子治疗的患者对化疗的耐受性可能增加。 4. 在治疗期间和之后,患者可以维持其当前的生活质量。
5. 有时它可以有效地用于治疗已经接受过辐射治疗的区域。
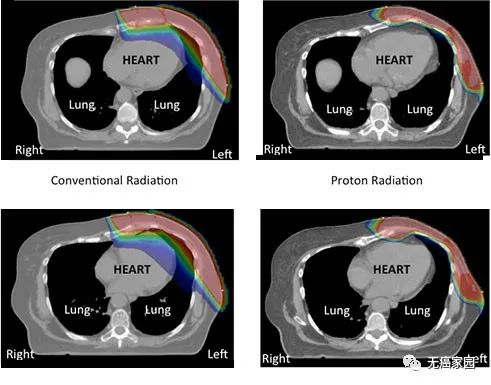
疗效相似,副作用更小首选质子治疗
患有乳腺癌的患者采取放疗是不可避免的治疗选择,然而放疗会造成一些皮肤红肿、脱发、照射部位疼痛、恶心等短期副作用,治疗结束或者对症处理后即可恢复。但是,肺炎、心脏毒性等严重并发症需引起注意。无癌家园的专家建议,在治疗早期乳腺癌时,质子治疗不失为一种比标准放射治疗更安全的替代方案。 乳腺癌患者可能受益于质子治疗辐射,这可以减少对心脏和肺部的辐射。质子治疗的高能量质子射束只会进入肿瘤,不会伤到周围正常细胞,更不会危及邻近的心脏器官,让乳腺癌治疗,不再担忧心脏损伤的问题。
03 乳腺癌21基因检测
乳腺癌多基因检测可帮助患者进行个性化全身辅助治疗以及预测患者的复发风险,而2019年乳腺癌NCCN指南强烈推荐考虑21基因检测。
乳腺癌21基因检测适合处于Ⅰ或Ⅱ期、雌激素受体阳性、淋巴结转移阴性、将要采用他莫昔芬治疗的新确诊患者;绝经后淋巴结阳性、雌激素受体阳性的侵润性患者,也可以通过21基因检测确定化疗获益。
04 术后辅助化疗
对患者基本情况(年龄、月经状况、血常规、重要器官功能、有无其他疾病等)、 肿瘤特点(病理类型、分化程度、淋巴结状态、HER2及激素受体状况、有无脉管瘤栓等)、治疗手段(如化疗、内分泌治疗、靶向药物治疗等)进行综合分析,医师根据治疗的耐受性、术后复发风险、肿瘤分子分型和治疗敏感度选择相应治疗,并权衡治疗给患者带来的风险-受益,若接受化疗的患者受益有可能大于风险,可进行术后辅助化疗。
术后辅助化疗适应证
1. 浸润性肿瘤大于2cm
2. 淋巴结阳性
3. 激素受体阴性
4. HER-2阳性(对T1a以下患者目前无明确证据推荐使用辅助化疗)
5. 组织学分级3级
辅助化疗方案
1)首选含蒽环类药物联合或序贯化疗方案:
以蒽环类为主的方案,如CA(E)F、A (E)C、FEC方案(C:环磷酰胺,A:多柔比星,E:表柔比星,F:氟尿嘧啶)。
蒽环类与紫杉类联合方案,例如TAC(T:多西他赛)。
蒽环类与紫杉类序贯方案,例如AC→T/P(P:紫杉醇)或FEC→T。
2)不含蒽环类的联合化疗方案,适用于老年、低复发风险、存在蒽环类禁忌或不能耐受的患者,常用TC方案。
3)一般根据术后复发风险,选择不同的辅助化疗方案。
高危患者,倾向于选择含蒽环和紫杉的方案,例如:AC-T、FEC-T、TAC、密集化疗AC-P等;
中危患者,倾向于单含蒽环或单含紫杉的方案,例如:CAF、CEF、TC(6周期)等;
需要化疗的低危患者,可选择4-6周期的单含蒽环或非蒽环方案,例如AC、EC、TC等。
4)三阴性乳腺癌,除部分肿瘤负荷较小的患者外(如T1,N0),一般推荐A(E)C-T(P)的化疗方案,剂量密集型A(E)C-T(P)方案可优选用于部分可耐受的三阴性乳腺癌患者。
5)大多数Luminal B 乳腺癌患者需要接受术后辅助化疗,方案应包含蒽环和(或)紫杉类。
6)LuminalA型乳腺癌对化疗反应较差,如淋巴结1-3个阳性可选择4~6周期的A(E)C或TC方案,但对淋巴结转移≥4个的高危患者,可推荐A(E)C-T(P)方案。
05 术后辅助内分泌疗法
内分泌疗法 内分泌疗法又称为激素疗法。大多数雌激素或孕激素受体呈阳性反应患者是由于激素来促进肿瘤生长,因此阻断激素可以帮助预防癌症复发和促进乳腺癌细胞死亡。 对于晚期患者,内分泌治疗一般需要持续5到10年,以保证完全杀灭肿瘤细胞。由于这类是乳腺癌患者中的大多数,而且治疗效果不错,因此乳腺癌整体存活率比较高。
目前FDA批准的内分泌治疗药物:
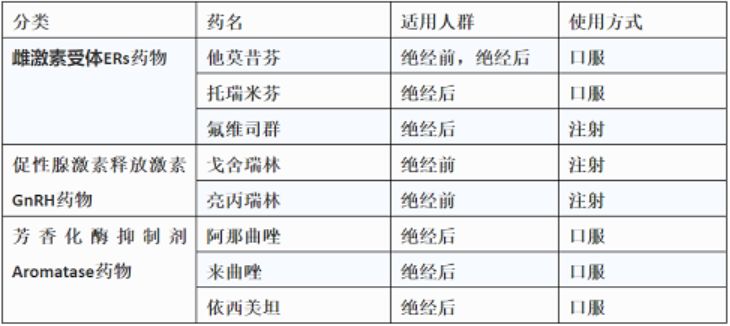
通过上面的表格我们可以看出,绝经前和绝经后的患者使用的治疗方案是不同的。
绝经前
他莫昔芬联合或不联合治疗。
由于卵巢也会产生雌激素,所以有些情况下医生会建议摘除卵巢。
芳香酶抑制剂治疗以阻止或减少卵巢产生多少雌激素,或对卵巢采取放射治疗。
绝经后
芳香化酶抑制剂联合或不联合化疗。
芳香酶抑制剂治疗后使用他莫昔芬联合或不联合h化疗。
06 靶向治疗
如果患者不幸乳腺癌复发,还可以选择采用靶向治疗。靶向治疗是在细胞分子水平上,针对已经明确的致癌位点(癌细胞内部的一个蛋白分子、或一个基因片段)进行治疗。靶向药物的研发和应用使得癌症患者的治疗模式发生变化,极大地延长了患者的生存期。但每个患者的突变基因不同,同一种靶向药,不能用于所有患者。为了判断患者是否可使用靶向治疗药物,首先需要进行基因检测,通过基因检测,确定患者致癌位点,然后再选择合适的靶向药。
与化疗不同,靶向治疗可阻止癌细胞的生长和扩散,同时限制对健康细胞的损害。
靶向治疗前需要进行基因检测找到特定分子靶标,首个被批准的乳腺癌靶向治疗是抗HER2的靶向药曲妥珠单抗。
目前已获得FDA批准的药物如下:
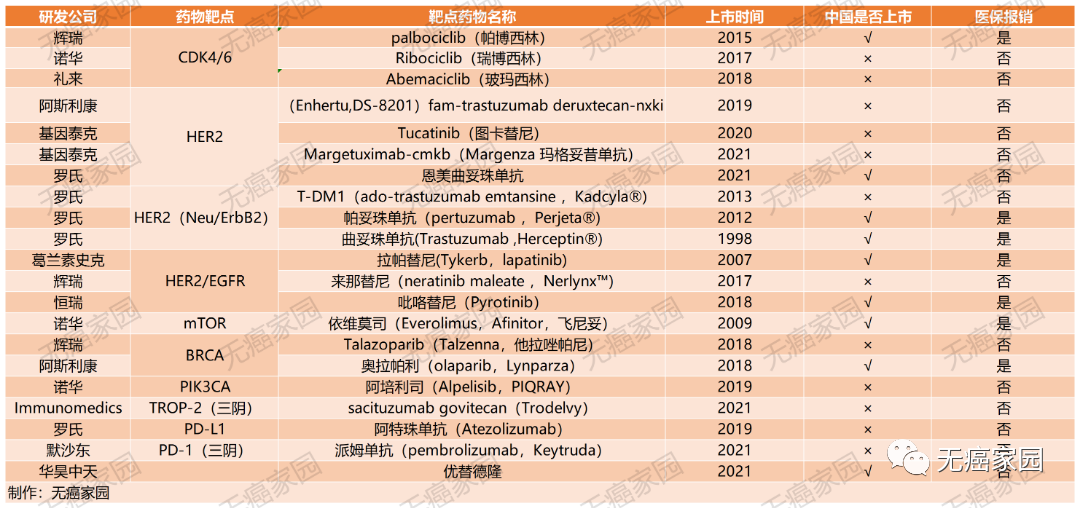
对于HER2阳性乳腺癌,其实肿瘤患者们有更多选择。
就在2021年1月,FDA授予全新抗体偶联药物ARX788快速通道指定,旨在加速这一先进抗癌疗法的上市进程,为一线治疗后进展的晚期HER2阳性乳腺癌患者带来更好的治疗选择。这也是ARX788的一个重要里程碑,期待ARX788尽快获得FDA批准早日上市。
这项临床试验结果在2020年12月的圣安东尼奥乳腺癌研讨会上公布,值得一提的是,这项在中国HER2阳性乳腺癌1期试验中,客观缓解率高达 74%,其中19名患者中有14名有响应,疾病控制率高达100%。
在美国和澳大利亚进行的1期HER2阳性泛肿瘤试验中,客观缓解率为67%,3名患者中有2名有反应,疾病控制率为100%。
07 免疫疗法
免疫疗法 免疫疗法,也称为生物疗法,旨在增强人体对抗癌症的天然防御能力。
目前FDA批准了两款用于乳腺癌的免疫疗法:
Atezolizumab(Tecentriq):在2019年,美国食品药品监督管理局(FDA)批准了atezolizumab联合蛋白结合的紫杉醇(见上文化学疗法)用于局部晚期三阴性乳腺癌,不能通过手术和转移性三阴性乳腺癌切除。此外,仅批准用于PD-L1检测呈阳性的乳腺癌。
派姆单抗(Keytruda):这是FDA批准用于治疗转移性癌症或无法通过手术治疗的癌症的一种免疫疗法。这些肿瘤还必须具有称为微卫星不稳定性高(MSI-H)或DNA失配修复缺陷(dMMR)的分子改变。
08 调动免疫军团调节免疫
肿瘤患者的免疫功能本身处于失常状态,而手术,放疗,化疗会对人体的免疫功能造成一定损伤,在临床治疗后,尽快调整免疫功能是预防复发转移的重中之重。 免疫功能的调节除了可以通过饮食,运动等日常生活方式,还需要临床治疗尽快帮助我们恢复,如注射胸腺肽类的药物、干扰素,以及恢复免疫试别功能和恢复免疫杀伤功能的各类细胞免疫回输等。
CAR-T(嵌合抗原受体T细胞)疗法
自从肿瘤免疫治疗成为第四种癌症治疗方法,研究者们逐渐将目光投向近几年来的热门疗法——CAR-T疗法。
CAR-T疗法就是嵌合抗原受体T细胞免疫疗法,是一种治疗肿瘤的新型精准靶向疗法。 通过基因工程技术将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞这个普通“战士”改造成 “超级战士” ,即CAR-T细胞, 专门识别体内肿瘤细胞,并高效杀灭肿瘤细胞 ,从而达到治疗恶性肿瘤的目的。
2018年圣安东尼奥乳腺癌研讨会上,根据正在进行的I期研究的结果。CAR-T治疗晚期三阴乳腺癌(TNBC)获得了长期病情稳定。
西雅图华盛顿大学医学博士Jennifer Specht提供了7名表达ROR1的三阴性乳腺癌(TNBC)患者的数据。
所有接受治疗的患者(年龄27~67岁)至少有3线既往转移治疗的经历。3名患者接受多达9个前线治疗(1线代表一种方案,治疗无效换另一种方案,即2线,3线……),1名11个前线治疗。
最后的结果也令人惊喜,经CAR-T治疗后,患者的病情持续时间延长,一个达15周,另一个达19周,没有任何后续治疗方案的治疗效果超过CAR-T细胞。
另外,有一个患者第一次回输CAR-T后病情稳定,第二次回输后部分应答持续14周之久(对于晚期三阴乳腺癌,延长1周生存期就很不容易了!!)。
NK细胞疗法
除了CAR-T疗法外,还有我们熟知的NK细胞(自然杀伤细胞),其在肿瘤免疫治疗方面大有可为。目前用于肿瘤免疫治疗的NK细胞策略有:体外活化的自体或异体NK细胞治疗;联合NK细胞和单抗药(如免疫检查点抑制剂)来诱导抗体特异的细胞毒性;构建CAR-NK细胞免疫疗法。
树突细胞疫苗
树突细胞是目前所知的机体内功能最强的抗原提呈细胞,最大的特点是能够刺激初始T细胞进行增殖。因此,DC是机体免疫应答的始动者,在免疫应答的诱导中具有独特的地位。树突细胞在体内充分激活T细胞,促进T细胞对肿瘤的清除,树突细胞还能促进T细胞富集,增强对T细胞激活。
DC疫苗已经被国际医学抗肿瘤领域广泛认可,并已经应用于多种癌症的临床治疗中,这是癌症患者治疗的新希望。此外,德国、日本也有树突细胞疫苗用于临床辅助治疗多种癌症,如肺癌、肝癌、肾癌、乳腺癌、皮肤癌等。
CTL(细胞毒性T淋巴细胞)疗法
对于广大的无法手术的晚期癌症患者,什么细胞疗法可以作为辅助治疗呢?
近年来,针对这部分患者,研究者们一直在研发新的免疫治疗方案,其中就有CTL(cytotoxic T lymphocytes)技术,即细胞毒性T淋巴细胞。该技术主要是利用癌细胞特有的、正常细胞上没有或者含量很低的蛋白质做诱饵,把外周血中那“万里挑一”的真正能抗癌的淋巴细胞,挑选出来,然后在体外进一步改良和扩增,然后回输给患者。
MTCA-CTL免疫疗法是国内推出的新一代生物免疫治疗模式。在保证非MHC限制性杀伤性NK-T细胞扩增的同时,定向扩增HC限制性的CD8+特异性CTL细胞,使其在细胞产品中的比率可达到60%~70%。这种杀伤细胞的共同作用,使杀伤肿瘤细胞的效率更高。
目前正在中国医学科学院肿瘤医院进行二期临床试验的多靶点复合抗原肽生物免疫治疗技术,是第五代也是全新一代细胞免疫治疗技术,可优化DC(树突细胞)活化方法,以增强免疫细胞对肿瘤细胞的杀伤作用,目前已取得很好的临床效果,相信将真正的让癌症患者受益。
【主要适用于实体肿瘤】头颈部肿瘤、食道癌、肺癌、胃癌、乳腺癌、肝癌、膜腺癌、结亘肠癌、卵巢癌、子宫癌、彗癌、前列腺癌、恶性黑色素瘤、肉瘤、部分恶性淋巴瘤。
定期随访和复查
术后局部复发,大部分在2年之内发生,其中约有40%发生在术后6个月以内。手术过后切勿万事大吉,6个月内最好每月去复查1次,6~12个月内每2个月复查1次,1~2年每3个月复查1次;2年以上每半年复查1次。
同时患者还可进行自我检查,经常触摸患侧胸壁、对侧乳房、双侧腋窝及锁骨上窝等部位,若发现有可疑的肿块,应立即到医院检查。两年后复发的可能性相对较小,这时可每隔6个月或1年复查1次,以防远处转移。为了防止复发,医生会根据治疗方案开抗癌药物,患者除按时服药外,更要定期复查,检查这些药物是否对身体产生副作用,并及时调整用药种类及剂量。
乳腺癌复查手段
常规复查手段有:乳腺超声、血常规检查、血生化检查、 肿瘤标志物、腹部超声、骨密度、心脏彩超 非常规复查手段有:乳腺钼靶(1年1次)、胸部X线(1年1次)、 乳腺MRI(必要时)、骨扫描、PET-CT、头颅-CT 合理调养身体 如果乳腺癌患者术后身体较为虚弱,加之放化疗后的毒副反应严重,则应以卧床静养为主,不要急于起来活动。饮食上应选择比较容易消化、符合患者口味、富含各种维生素及微量元素的食物(如如海藻、青萝卜、木瓜、红薯、金针菇、大蒜、芹菜、绿花菜、大豆、猕猴桃、橘柑等),少食油腻食物。 如果患者术后一般状况尚好,但放化疗后出现骨髓抑制,即血细胞明显减少时,应尽量减少外出,避免与感冒患者接触,减少发生各种感染的机会;如血小板显著下降,还应避免外伤,避免各种出血倾向。 如果患者放化疗后出现厌食、恶心、呕吐等消化道反应,则应安排少食多餐,吃些清淡可口的食物,吞咽时小口细嚼慢咽,餐后不要平躺,宜半坐卧位,不宜立即活动。
注意功能锻炼
由于乳腺癌手术范围较大,局部皮肤、皮下脂肪、血、神经、淋巴管以及肌肉等都会有不同程度的损伤,从而影响患肢上肢的活动,甚至出现胸廓畸形。最重要的预防措施是及时进行功能锻炼。通常手术后1周左右就应该开始活动上肢,先使患侧手臂逐渐上举,开始时由于疼痛,活动度很小,但不要着急,要坚持天天练习。当患侧手臂可以触到同侧耳朵时,可练习用患侧手臂梳头,先从患侧梳起,逐渐梳向对侧,直到可以触到对侧耳朵。另外还可将患侧手臂背后逐渐向上摸,直到能摸到对策肩胛骨。
还可做些扩胸运动,使患侧胸廓及肩关节得到适当的运动。由于手术中患侧淋巴结被清扫,许多毛细血管、淋巴结被损伤,可能会影响上肢血液和淋巴液的回流,致使患侧上肢肿胀。预防这一点,除了要抬高手臂外,还应适当活动上肢,避免肌肉收缩,促进血液、淋巴液回流。若出现了上肢肿胀,则应尽量避免在患肢注射或静脉穿刺注射液。总之,只要及时并坚持锻炼,患肢手臂功能是完全可以恢复正常的。
远离致癌因素
乳腺癌患者术后要远离各种促进乳腺癌复发的因素。要做到不吸烟、不饮酒,少吃高脂肪、熏制和烧烤食品,避免使用含雌激素较高的美容化妆品,尽量避免接触放射性和电磁辐射。
最后,预防乳腺癌复发和转移还需要科学的生活方式。调整好生活节奏,避免和减少精神、心理紧张因素,保持乐观的情绪和良好的心态,积极参加体育锻炼,养成科学的饮食习惯等。