关于177Lu-LNC1008注射液
01
公司在研产品177Lu-LNC1008 注射液是一种靶向整合素alpha-v beta-3(αvβ3)蛋白的放射性体内治疗药物,拟用于治疗整合素alpha-v beta-3(αvβ3)阳性的晚期恶性实体瘤患者,目前在国际和国内尚无同靶点放射性治疗药物上市。
02
整合素αvβ3是一种重要的细胞表面受体,属于整合素家族,在肿瘤进展中发挥着重要的作用,参与包括肿瘤发生、上皮-间质转化(epithelial-mesenchymaltransition, EMT)、血管生成、肿瘤干性、代谢重编程、免疫逃逸、骨转移和耐药等多个相关进程。LNC1008前体能特异性地与整合素αvβ3结合,通过将放射性核素镥[177Lu]靶向运送至整合素αvβ3阳性的实体瘤处实现肿瘤的精准治疗。
03
177Lu-LNC1008注射液除了具有靶向治疗的优势外,通过加入专利化学结构能够改善探针的药代和药效性能,增加肿瘤对药物的有效摄取,延长治疗时间窗并可以在同等或更优的治疗效果下降低放射性核素的用量,进而降低患者的治疗成本。
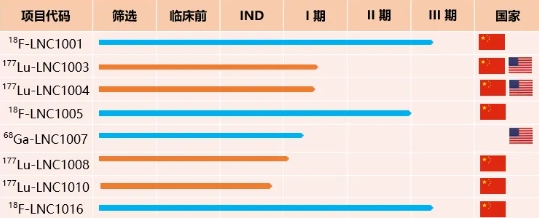
蓝纳成迄今已有涉及4个靶点共8款诊疗一体化创新核药,在中美分别处于临床试验或IND审评阶段,共计获得12项临床试验批件。4款诊断核药中,2款处于III期临床试验,1款处于I期临床研究阶段。4款治疗核药中,3款处于I期临床研究阶段,1款处于IND审评阶段。