作为肺癌临床分期的关键核技术手段,¹⁸F-FDG PET/CT在国内高炎症背景地区正面临特异性不足的重大挑战。最新研究揭示了其分子机制:恶性细胞与结核、结节病等引发的炎性细胞,均通过高表达葡萄糖转运蛋白(GLUT1/GLUT3)和己糖激酶,对放射性示踪剂¹⁸F-FDG呈现相似的、基于“Warburg效应”的高摄取,导致核医学影像上的“同像性”,常规SUVmax≥2.5阈值特异性可能低至12-40%。
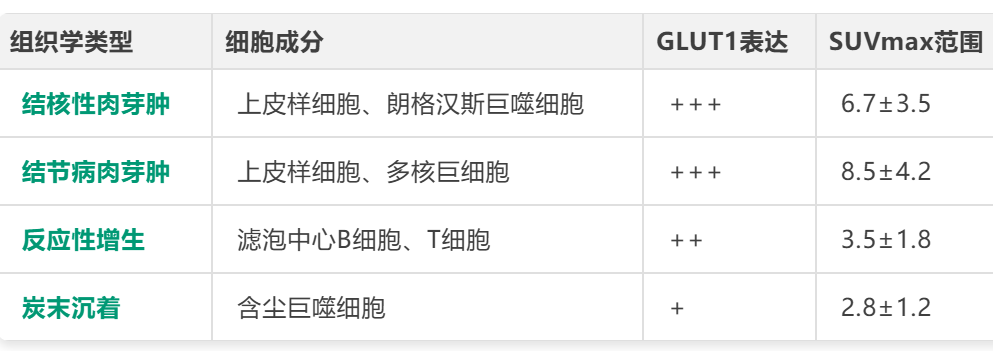
为提升这一核技术的诊断效能,核医学领域专家提出了一套综合优化方案。核心在于摆脱单一SUVmax阈值的局限,转向多参数核医学定量分析。策略包括:将诊断阈值根据流行病学背景个体化提升至SUVmax≥4.0-5.0;采用淋巴结/纵膈血池SUV比值(≥1.4)进行内部标准化;利用双时相扫描技术,通过计算SUV保留指数(RI≥10%)来捕捉恶性与炎症病灶在放射性示踪剂代谢动力学上的细微差异。同时,必须深度融合PET提供的代谢信息与同机CT的形态学特征(如短径、形态)进行综合评估。
研究明确强调,对于SUVmax在2.5-6.0这一核医学影像的“灰色地带”,最终的诊断金标准仍是超声支气管镜引导下经支气管针吸活检(EBUS-TBNA)的病理验证。这一系列基于核技术原理的优化策略,旨在显著提高¹⁸F-FDG PET/CT在复杂情况下鉴别良恶性的能力,从而为肺癌精准分期提供更可靠的核医学依据。