一项发表于《EJNMMI Research》的最新研究显示,重庆医科大学附属第一医院的庞华、王政杰教授团队,成功开发了一种基于肽核酸的预靶向策略,有望显著降低放射性核素治疗对正常组织的辐射损伤,提升治疗的安全性窗口。该研究利用铽-161(¹⁶¹Tb)这一核素,探索了其在肿瘤精准治疗中的新应用模式。
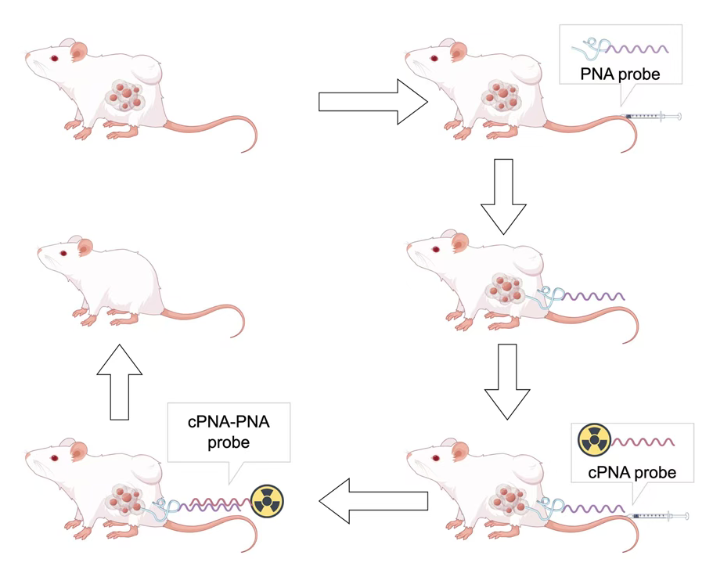
PNA介导的放射性预靶向治疗示意图
传统的放射性核素疗法,如直接将¹⁶¹Tb标记在靶向分子(¹⁶¹Tb-EB-RGD)上,虽能有效杀伤肿瘤,但因分子在血液循环中存留时间较长,导致血液等正常组织承受不必要的辐射。为解决此难题,该团队设计了一种精巧的“两步法”预靶向策略。第一步,先注射未经放射性标记的、由肽核酸修饰的靶向探针。该探针可借助RGD序列特异性地结合在肿瘤细胞表面,并在肿瘤部位“锚定”。第二步,等待足够时间让未结合的探针从正常组织清除后,再注射放射性核素¹⁶¹Tb标记的互补序列肽核酸。第二步的放射性分子通过与第一步“锚定”在肿瘤上的探针发生特异性杂交,从而将放射性精准、高效地带到肿瘤病灶,实现靶向杀伤。
研究表明,这种预靶向策略在4T1肿瘤模型中取得了显著效果。与常规的¹⁶¹Tb-EB-RGD直接疗法相比,预靶向策略(¹⁶¹Tb-cPNA-PNA-EB-RGD)将血液中的放射性摄取降低了32倍,极大地减少了全身辐射暴露。虽然肿瘤的绝对放射性摄取量有所降低,但其肿瘤与正常组织的靶向特异性比(如肿瘤/肌肉比)反而更高。在为期30天的治疗观察中,预靶向治疗组有效抑制了肿瘤生长,且小鼠体重稳定,未出现常规治疗组所见的体重显著下降等全身毒性反应,显示出卓越的治疗安全性。
该研究验证了基于肽核酸的预靶向平台与¹⁶¹Tb核素结合应用的可行性。其核心价值在于,通过功能模块的分离与有序递送,在维持有效抗肿瘤活性的前提下,大幅拓宽了放射性核素治疗的安全窗口。这一策略不仅为整合素αvβ3阳性的肿瘤提供了一种前景广阔的低毒治疗方案,其模块化设计思路也为开发其他靶向性更强、更安全的核素诊疗药物提供了新的技术范式。