11月11日,拜耳研发的1类放射性治疗药物“BAY 3547926 注射液”的临床试验申请获得国家药品监督管理局药品审评中心受理公开。
2025年4月29日,拜耳宣布启动海外I期试验,评估225Ac-GPC3(BAY 3547926)单药及联合疗法在晚期HCC患者中的安全性、耐受性和初步疗效,计划招募148名患者。
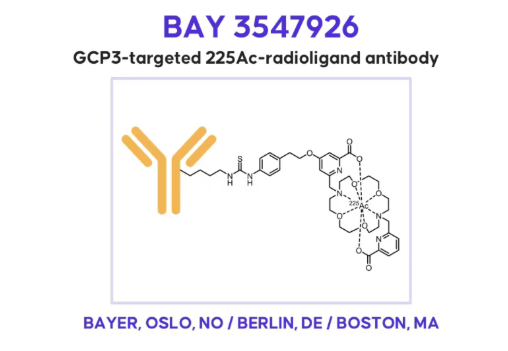
BAY 3547926 注射液采用单克隆抗体偶联Ac-225的技术路线,该药物是拜耳临床开发的第三个TAT项目,也是拜耳治疗HCC的第一个研究性靶向放射性药物。此次受理标志着BAY 3547926正式进入中国研发管线。作为拜耳首款针对肝癌的靶向放射性药物,其国内申报的推进,不仅契合中国肝癌高发的疾病负担需求,更体现了跨国药企在核药领域布局中国市场的战略考量。
拜耳是比诺华更早入局核药的跨国药企之一,2009年便与Algeta联合开发Xofigo(氯化镭223),2013年获批上市用于晚期骨转移型去势抵抗性前列腺癌。
Xofigo是全球首款且唯一一款获批的α粒子放射性药物,主要通过活性部位模拟钙离子,然后结合羟基磷灰石(HAP)沉积区域发挥治疗作用。
自2013年上市后,Xofigo销售额便稳步上升,2017年达到4.71亿美元。
不过,虽然Xofigo将核药重新带到了大家的视线中,但它毕竟属于传统放射性治疗药物,在前列腺癌展现出的疗效不适用也不能转化为其他癌症治疗,开发前景和市场空间有限,因此未能引起企业的广泛跟进。
此后,拜耳又大手笔收购Algeta、Noria和PSMA Therapeutics继续加磅RDC,进一步加强了其在核药领域的研发和市场影响力。